
Множественная миелома

Множественная миелома (ММ) — это B-клеточная злокачественная опухоль, морфологическим субстратом которой являются плазматические клетки, продуцирующие моноклональный иммуноглобулин1.
Эпидемиология1
Множественная миелома (ММ) — это В-клеточная злокачественная опухоль, морфологическим субстратом которой являются плазматические клетки, продуцирующие моноклональный иммуноглобулин. ММ составляет приблизительно 1% среди всех злокачественных опухолей, 13% среди гемопоэтических опухолей. В России в 2017 году впервые диагностировано 4 075 случаев, умерло 2 587 больных. Заболеваемость ММ в России составила 2,8 на 100 тысяч, возрастная медиана заболеваемости 63,7 года.
Диагностика ММ1
При установлении диагноза симптоматической ММ должны присутствовать следующие критерии:
Плазматические клетки в костном мозге 10% и более и/или
Плазмоклеточная опухоль в биопсийном материале пораженной ткани в сочетании со следующими признаками:
Один или более признаков поражения органов или тканей, связанных с плазмоклеточной пролиферацией (симптомокомплекс CRAB):
Calcium — гиперкальциемия (> 11,5 мг/дл [> 2,65 ммоль/л]),
Renal — почечная недостаточность (клиренс креатинина < 40 мл/мин, креатинин > 2 мг/дл [> 177 мкмоль/л]),
Anemia — анемия (Hb < 10 г/дл или на 2 г/дл ниже нормального уровня Hb),
Bone — поражение костей (один или более остеолитический очаг, выявленный при рентгенографии, компьютерной томографии (КТ) или позитронно-эмиссионной томографии (ПЭТ/КТ)).
Или один или более признаков опухолевой активности
>60% плазматических клеток в костном мозге
Соотношение вовлеченных/невовлеченных свободных легких цепей иммуноглобулинов сыворотки (СЛЦ)>100
>1 очага поражения по результатам МРТ, размер очага должен быть не менее 5 мм
Стадирование ММ1, 2, 3
Стандартные факторы риска ММ и пересмотренная Международная система стадирования (R-ISS)
Прогностический фактор | Критерии |
Стадия ISS | |
I | β2-микроглобулин сыворотки < 3,5 мг/мл и сывороточный альбумин ≥ 3,5 г/дл |
II | β2-микроглобулин сыворотки < 3,5 мг/мл и сывороточный альбумин < 3,5 г/дл или β2-микроглобулин сыворотки 3,5-5,5 мг/мл независимо от уровня альбумина |
III | β2-микроглобулин сыворотки ≥ 5,5 мг/мл |
Цитогенетические аномалии, выявленные методом FISH | |
Высокий риск | Наличие del17p и/или t(4;14) и/или t(14;16) |
Стандартный риск | Отсутствие цитогенетических аномалий высокого риска |
Уровень ЛДГ | |
Норма | ЛДГ в границах нормальных значений |
Высокий уровень | ЛДГ сыворотки выше верхней границы нормального уровня |
Новая модель стратификационного риска ММ Стадии R-ISS | |
I | ISS стадия I, стандартный цитогенетический риск по FISH, нормальный уровень ЛДГ |
II | Критерии не соответствуют I или III стадии R-ISS |
III | ISS стадия III, высокий цитогенетический риск по FISH, высокий уровень ЛДГ |
Основной алгоритм терапии множественной миеломы в РФ4
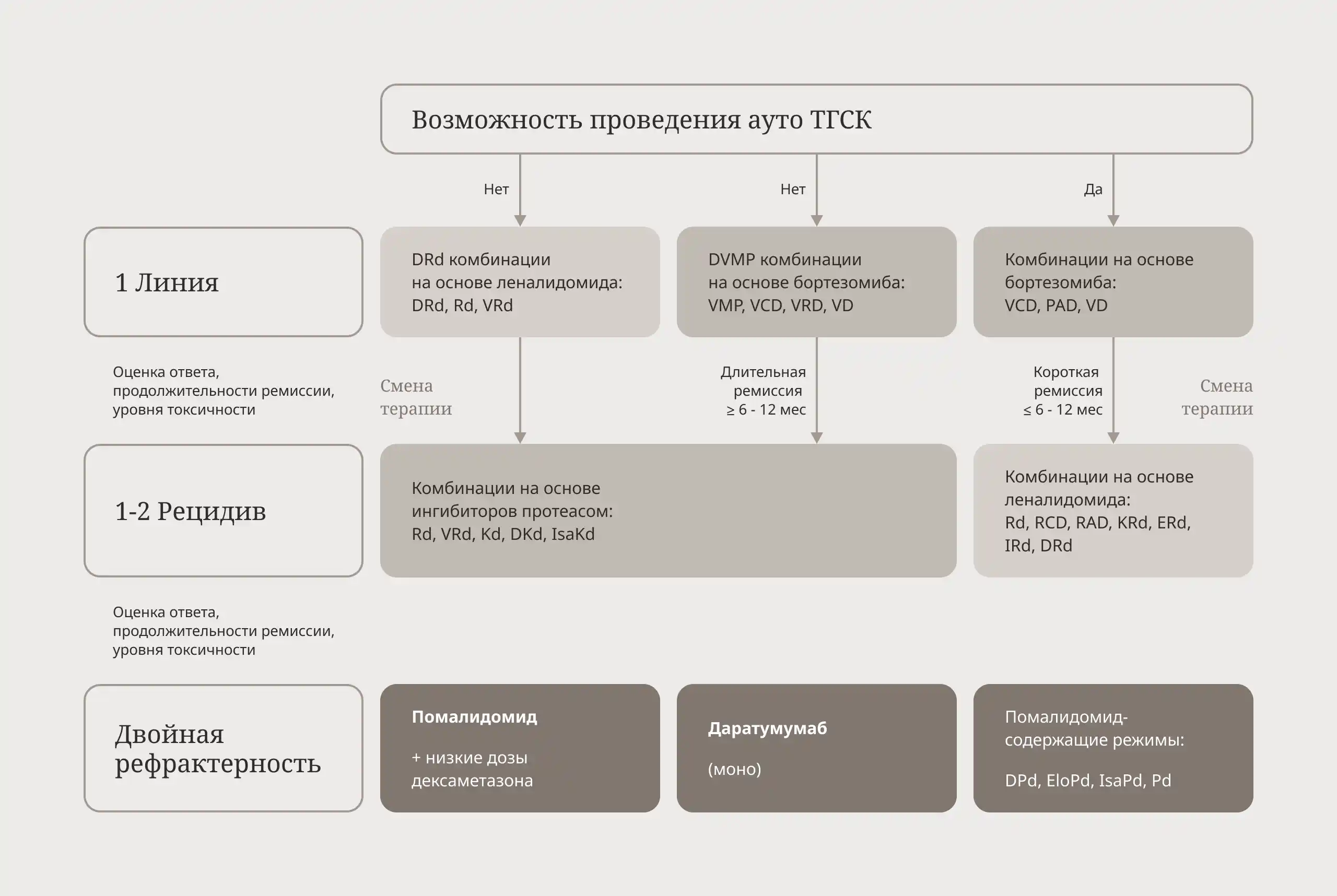
Оценка ответа на терапию1, 5
Международные критерии оценки, пересмотренные в 2011 году
Глубина ответа | Критерии |
Полная молекулярная ремиссия | Строгая ПР плюс отсутствие аберрантного клона в костном мозге при анализе 1 млн клеток методом проточной цитофлуометрии (> 4 цветов) |
Строгая ПР | ПР при нормальном соотношении СЛЦ и отсутствии клональных плазматических клеток в костном мозге по данным иммуногистохимического или иммунофенотипического методов |
ПР |
|
ОХЧР | М-протеин в сыворотке крови и моче определяется только при иммунофиксации, но не при электрофорезе, или отмечается снижение уровня М-протеина в сыворотке на 90% и более, а М-протеина в моче — до уровня менее 100 мг/сутки |
ЧР | М-протеин в сыворотке должен уменьшиться на 50% и более, в моче — на 90% и более (абсолютное количество М-протеина в моче должно быть менее 200 мг/сутки) |
Прогрессия заболевания | Повышение уровня М-протеина на 25% и более от наименьшего достигнутого уровня (в сыворотке увеличение на ≥5 г/л, в моче увеличение ≥200 мг/сутки)
|
Рецидивирующая/рефрактерная миелома | Рецидив заболевания во время терапии или прогрессирование заболевания в пределах 60 дней после самой последней терапии |
Определение и оценка минимальной остаточной болезни (МОБ)6
Под минимальной остаточной болезнью (МОБ) понимают популяцию опухолевых клеток, оставшуюся в организме после достижения клинико-гематологической ремиссии и недоступную для обнаружения с помощью обычного морфологического исследования7.
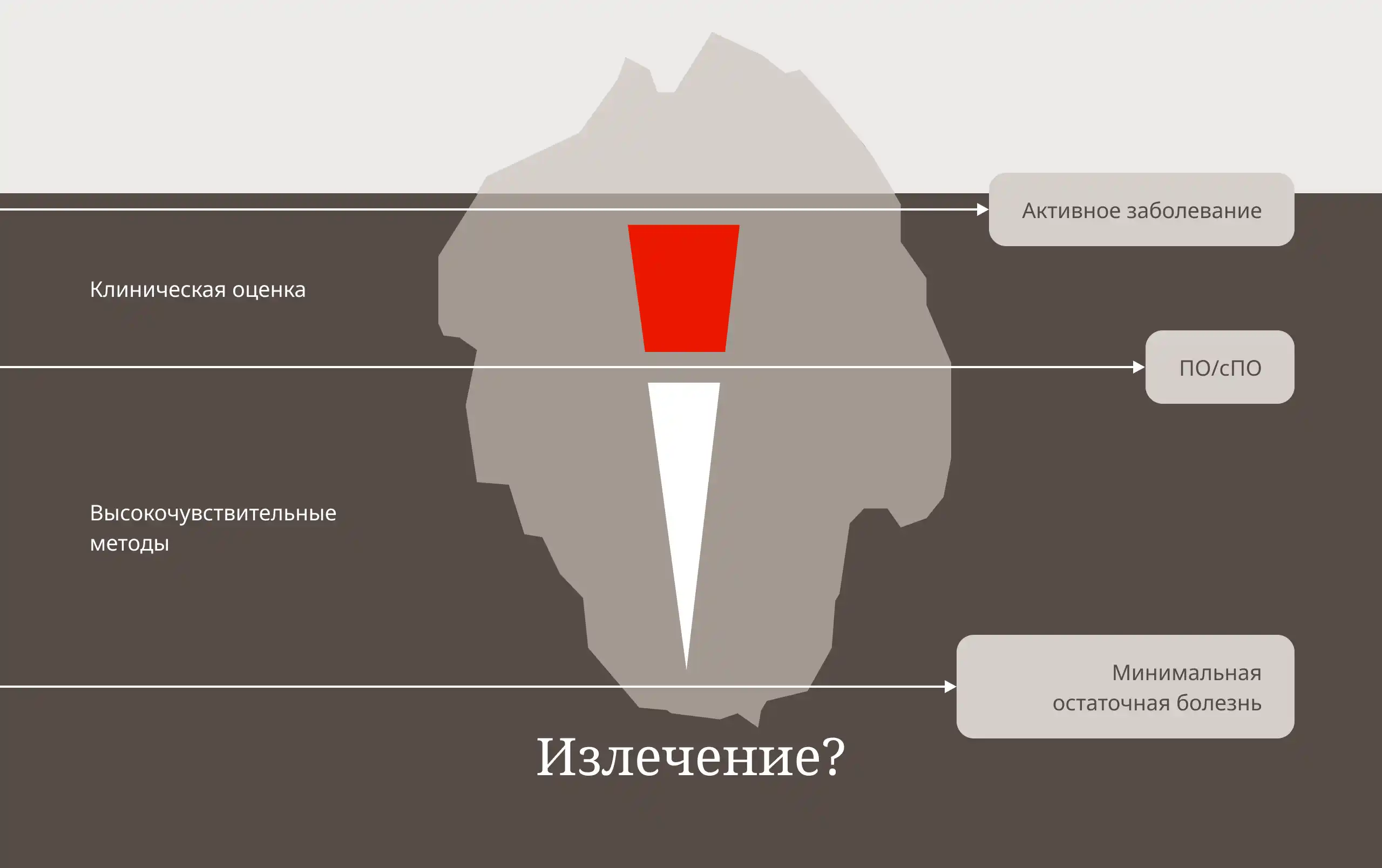
Пределы выявления опухолевого процесса
Методы определения МОБ6, 7, 8, 9
| Полимеразная цепная реакция (ПЦР) | Проточная цитометрия | Секвенирование нового поколения |
Возможность применения | 60-70% | Около 100% | ≥90% |
Необходимость исследования первичного образца | <1 млн клеток Могут быть использованы как замороженные, так и свежие образцы | >5 млн клеток Могут быть использованы только свежие образцы в течение 24-48 ч | <1 млн клеток Могут быть использованы как замороженные, так и свежие образцы |
Чувствительность теста | ≥1 в 10-5 | ≥1 в 10-5 | ≥1 в 10-5 |
Дополнительная информация, получаемая при анализе | Нет | Подробная информация о популяциях лейкоцитов и их относительном распределении | Информация о структуре гена иммуноглобулина В-клеток в исследуемых образцах пациентов |
Оборот и сложность метода | Трудоемкий; требует разработки специфичных для пациента праймеров/зондов; может занять несколько дней | Может быть сделан через несколько часов; автоматическое программное обеспечение | Может потребоваться несколько дней для исследования; требует интенсивной поддержки биоинформатики |
Стандартизация | EuroMRD | Выполнена EuroFlow consortium | В процессе |
Доступность | Повсеместно | Повсеместно | Только в исследовательских лабораториях |
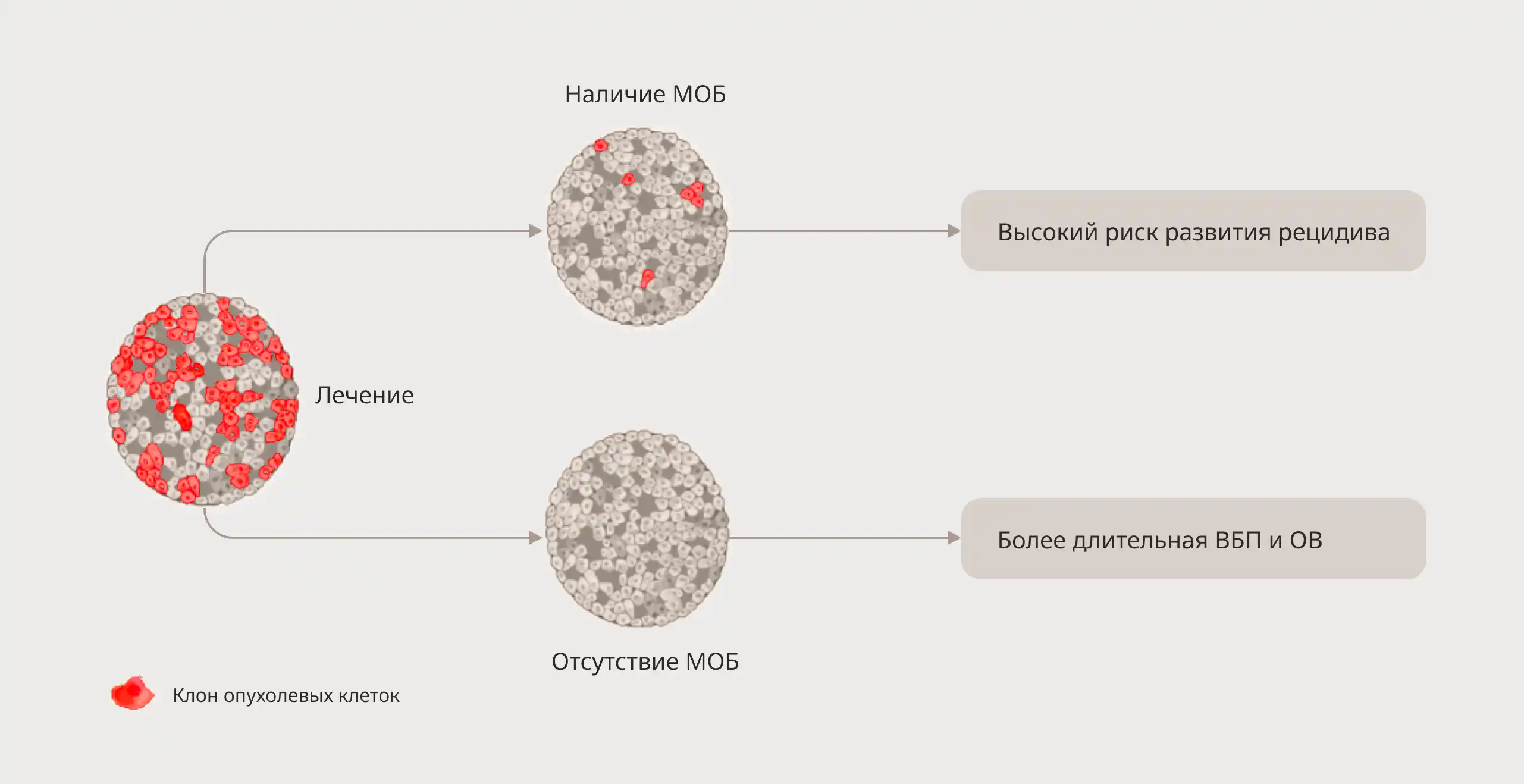
МОБ при множественной миеломе4
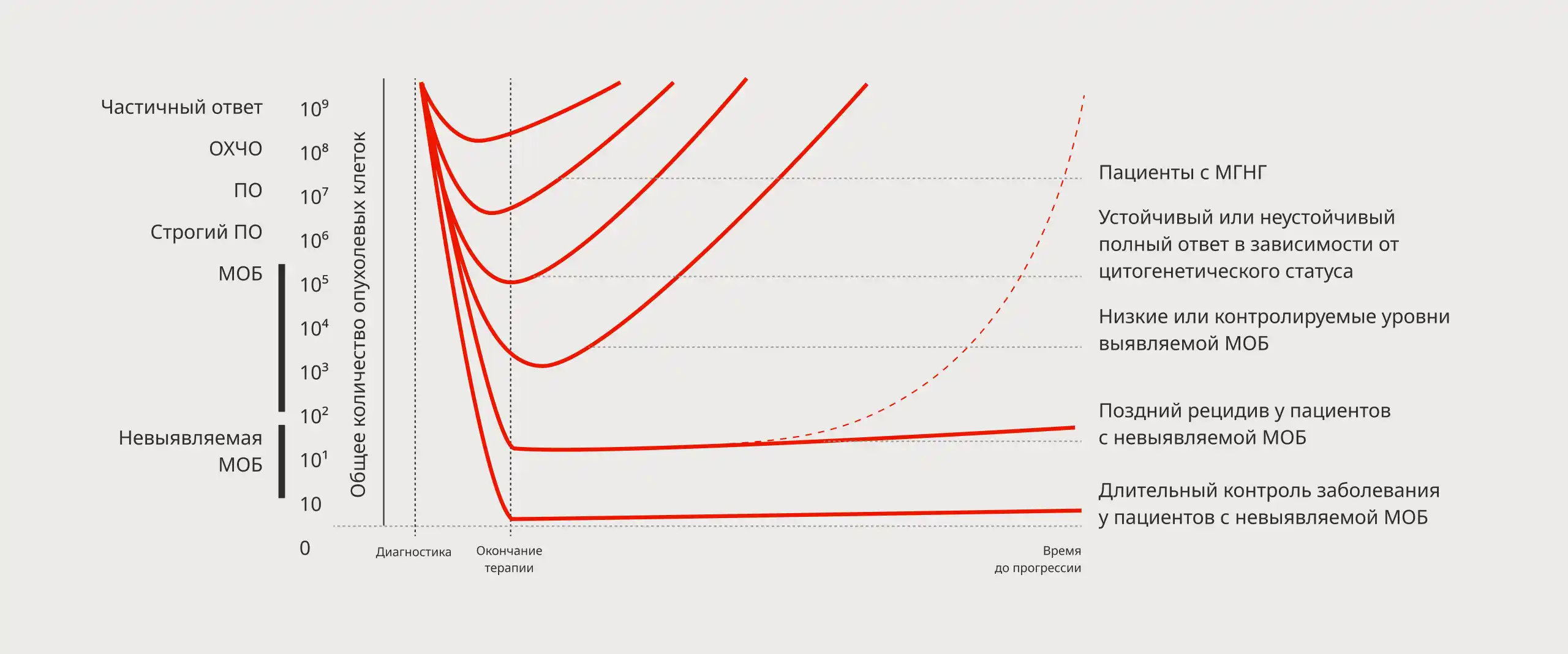
Оценка МОБ при помощи ультрачувствительных методов позволяет выявить опухолевый процесс задолго до появления клинических проявлений.
Пределы выявления опухолевого процесса
Влияние МОБ на прогноз заболевания9
Посмотрите видео о МОБ
Критерии IMWG по определению ответа на терапию с учетом МОБ (2016)8
Устойчивая МОБ-негативная ремиссия | МОБ «-» в костном мозге методом секвенирования нового поколения и/или проточной цитометрии нового поколения и методом ПЭТ-КТ, подтвержденная с интервалом в 1 год или более |
МОБ-негативная ремиссия, подтвержденная методом иммунофенотипирования | Отсутствие фенотипических аберрантных клональных плазматических клеток в костном мозге, определенных с помощью проточной цитометрии нового поколения с использованием стандартной процедуры EuroFlow для обнаружения МОБ при ММ (или одобренного эквивалентного метода) с минимальной чувствительностью 1×10-5 ядросодержащих клеток или выше |
МОБ-негативная ремиссия, подтвержденная методом секвенирования | Отсутствие клональных плазматических клеток в костном мозге, определяемых методом секвенирования нового поколения с использованием платформы LymphoSIGHT (или подтвержденный эквивалентный метод) с минимальной чувствительностью 1×10-5 ядросодержащих клеток или выше |
МОБ-негативная ремиссия, подтвержденная методом иммунофенотипирования и ПЭТ-КТ или методом секвенирования и ПЭТ-КТ | МОБ «-» в костном мозге методом секвенирования нового поколения или проточной цитометрии нового поколения и исчезновение каждой области повышенного поглощения препарата, обнаруженного в исходном состоянии или на предыдущей ПЭТ-КТ, или снижение метаболической активности, измеренной значением стандартизированного накопления до уровня менее, чем в средостении или окружающих нормальных тканях |
Сложности, перспективы на будущее и вопросы, связанные с МОБ, в терапии пациентов с ММ
Отсутствие стандартизации между лабораториями
МОБ должна определяться не только в ведущих научных центрах
Исследование МОБ должно быть выполнимым для большинства пациентов
Отсутствие четких рекомендаций по частоте выполнения оценки МОБ

Появление более чувствительных методов оценки МОБ
Накопление опыта по оценке МОБ
Данные текущих исследований помогут внедрить МОБ в клинические исследования и рутинную практику
Анализ МОБ может изменить подходы к терапии множественной миеломы:
Менее интенсивное лечение, ограничение его длительности
Ускоренное одобрение лекарственных препаратов
Снижение затрат на лечение
Улучшение качества жизни пациентов

Какой уровень чувствительности (10-4, 10-5, 10-6) лучше всего коррелирует с клиническим результатом?
Какое время является оптимальным для выявления МОБ?
Для каких пациентов достижение отрицательного статуса МОБ должно стать целью терапии?
Нужно ли брать образцы из нескольких зон?
FISH — флюоресцентная in situ гибридизация
ISS — международная система стадирования
АутоТГСК — трансплантация аутологичных гемопоэтических стволовых клеток
ГСК — гемопоэтические стволовые клетки
ЛДГ — лактатдегидрогеназа
ММ — множественная миелома
МОБ — минимальная остаточная болезнь
ОХЧР — очень хорошая частичная ремиссия
ПР — полная ремиссия
СЛЦ — свободные легкие цепи
ЧР — частичная ремиссия
Использованная литература
- 1
Anderson K.C., et al. Clin Cancer Res. 2017;23(15):3980-3993.
- 2
Yanamandra U., Kumar SK. Leuk Lymphoma. 2017:1-13.
- 3
Anderson K.C. Blood Adv. 2017;1(8):517-521.
- 4
Клинические рекомендации Множественная миелома, 2024.
- 5
Gormley N.J., et al. Cytometry B Clin Cytom.
- 6
Durie B.G., et al. Leukemia, 20 (2006), pp. 1467-1473.
- 7
Munshi N.C., et al. JAMA Oncol. 2017 Jan 1;3(1):28-35. doi: 10.1001/jamaoncol.2016.3160.
- 8
Paiva B., van Dongen J.J., et al. Blood 2015;125(20):3059-3068.
- 9
Kenneth C. Anderson, Daniel Auclair, Gary J. Kelloff. The role of MRD. Clin Cancer Res; 23(15) August 2017.
- 10
Sonneveld P. Blood Adv. 2017;1(8):522-525.
- 11
Kumar S., et al. Lancet Oncol. 2016 Aug;17(8):e328-e346. doi: 10.1016/S1470-2045(16)30206-6.
- 12
Ajoy Lawrence Dias and Dharamvir Jain. Cardiovasc Hematol Agents Med Chem. 2013 Dec; 11(4): 265-271.
- 13
Thompson M., et al. JAMA Oncol. 2018 Mar 1;4(3):394-400.